資源簡介
資源簡介
(共30張PPT)
第七章 有機化合物
第三節 乙醇 乙酸
第1課時 乙醇
環節一:情境導入,感知乙醇的物理性質
酒文化
歡時-----李白說:人生得意須盡歡,莫使金樽空對月。
古往今來,人們愛酒,愛它個中的滋味,更愛它帶給我們的精神慰藉。
喜時-----杜甫說:白日放歌須縱酒,青春作伴好還鄉。
離時-----王維說:勸君更盡一杯酒,西出陽關無故人。
愁時-----李白說:抽刀斷水水更流,舉杯消愁愁更愁。
環節一:情境導入,感知乙醇的物理性質
酒文化
環節一:情境導入,感知乙醇的物理性質
酒文化
環節一:情境導入,感知乙醇的物理性質
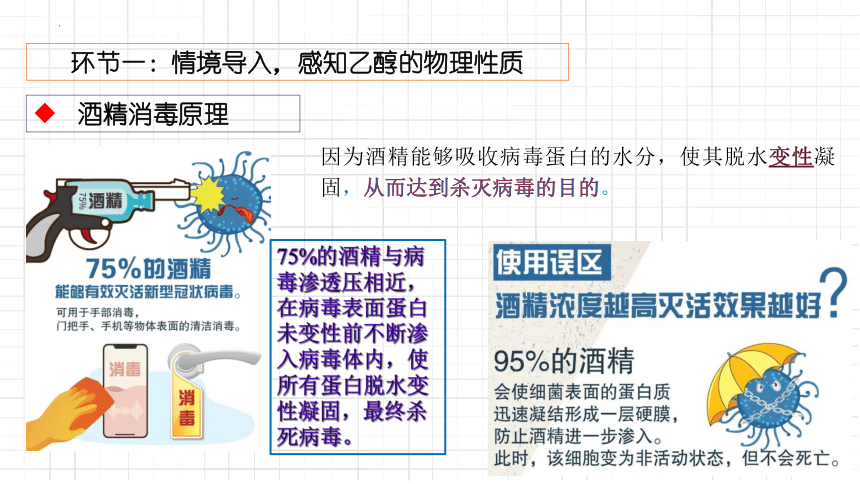
酒精消毒原理
因為酒精能夠吸收病毒蛋白的水分,使其脫水變性凝固,從而達到殺滅病毒的目的。
75%的酒精與病毒滲透壓相近,在病毒表面蛋白未變性前不斷滲入病毒體內,使所有蛋白脫水變性凝固,最終殺死病毒。
環節一:情境導入,感知乙醇的物理性質
乙醇的物理性質
無色、特殊香味液體
和水任意比互溶
易揮發
比水小
顏色、狀態、氣味
溶解性
密度
揮發性
俗稱:酒精
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
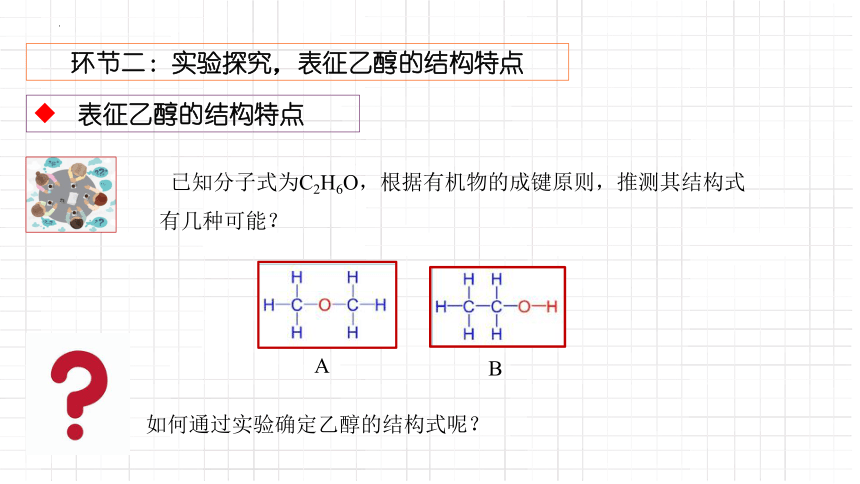
已知分子式為C2H6O,根據有機物的成鍵原則,推測其結構式有幾種可能?
B
A
如何通過實驗確定乙醇的結構式呢?
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
【實驗7-4】
在盛有少量無水乙醇的試管中,加入一小塊新切的、用濾紙吸干表面煤油的鈉,在試管口迅速塞上帶尖嘴導管的橡膠塞,用小試管收集氣體并檢驗其純度,然后點燃(如圖7-19),在將干燥的小燒杯罩在火焰上。待燒杯璧上出現液滴后,迅速倒轉燒杯,向其中加入少量澄清石灰水。
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
鈉沉在乙醇的底部,
反應較緩慢,表面有氣體放出 氣體能燃燒,燃燒產物不能使澄清的石灰水變渾濁
實驗現象:
鈉與乙醇反應生成的氣體為H2
鈉密度大于乙醇
實驗結論:
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
浮在水面
熔成球形
發出嘶聲放出氣泡劇烈
先沉后浮
仍為塊狀
沒有聲音
放出氣泡
緩慢
2Na+2H2O = 2NaOH +H2↑
?
與水反應的比較
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
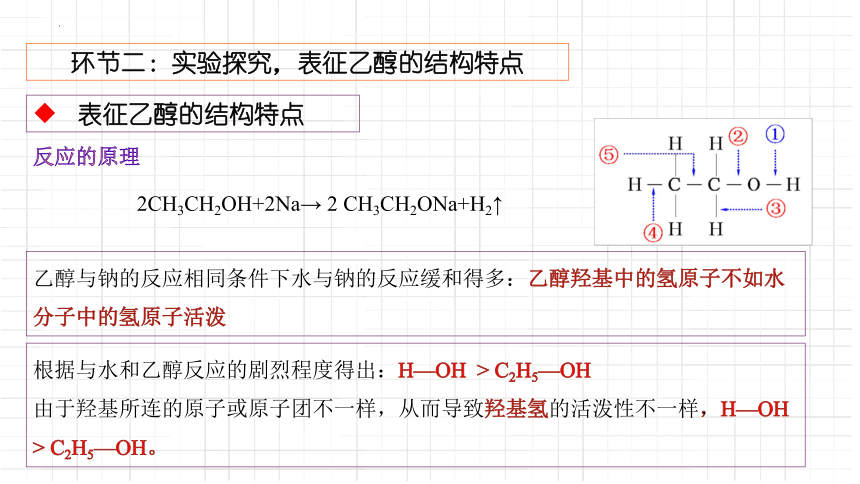
反應的原理
2CH3CH2OH+2Na→ 2 CH3CH2ONa+H2↑
乙醇與鈉的反應相同條件下水與鈉的反應緩和得多:乙醇羥基中的氫原子不如水分子中的氫原子活潑
根據與水和乙醇反應的劇烈程度得出:H—OH > C2H5—OH
由于羥基所連的原子或原子團不一樣,從而導致羥基氫的活潑性不一樣,H—OH > C2H5—OH。
環節二:實驗探究,表征乙醇的結構特點
表征乙醇的結構特點
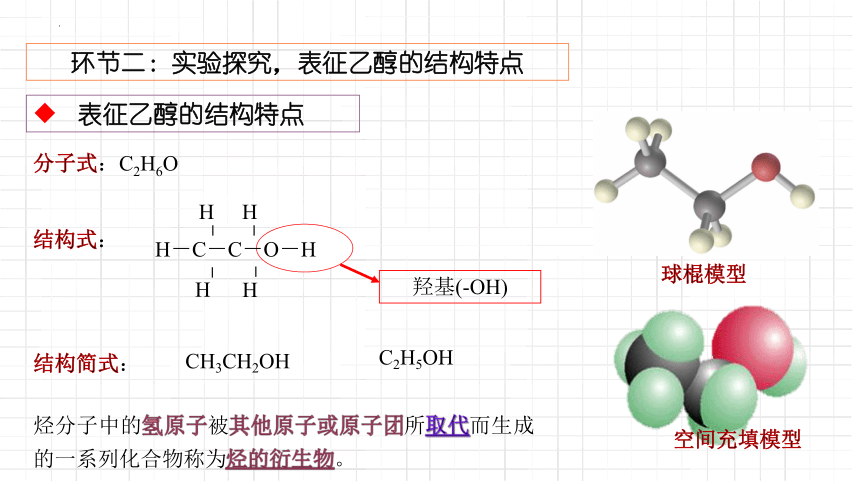
分子式:C2H6O
結構式:
結構簡式:
CH3CH2OH
C2H5OH
羥基(-OH)
H-C-C-O-H
-
H
-
-
-
H
H
H
球棍模型
空間充填模型
烴分子中的氫原子被其他原子或原子團所取代而生成的一系列化合物稱為烴的衍生物。
環節二:實驗探究,表征乙醇的結構特點
概念辨析
官能團:像這種決定有機化合物特性的原子或原子團叫做官能團。羥基是醇類物質的官能團,碳碳雙鍵和碳碳三鍵分別是烯烴和炔烴的官能團。
烴基:烴分子失去1個氫原子后所剩余的部分叫做烴基,可以用一R來表示。如一CH3叫甲基,一CH2CH3,叫乙基。
烴的衍生物:烴的衍生物分子一般可以看成是烴基和官能團相互結合組成的。例如,乙醇分子可以看成是由乙基和羥基組成的:CH3CH2-OH。
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
與鈉的反應
CH3CH2OH + Na → CH3CH2ONa + H2↑
2 2 2
H—C —C—O—H ,
H H
H H
①處O—H鍵斷開
①
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
氧化反應——燃燒
現象:產生淡藍色火焰,同時放出大量熱。
C2H5OH + 3O2 2CO2 +3H2O
點燃
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
氧化反應——催化氧化
高溫焊接銀器或銅器時,表面會生成黑色的氧化物,師傅說:把銅或銀器具趁熱蘸一下酒精,銅或銀會光亮如初!這是為什么呢?
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
【實驗7-5】 向試管中加入少量乙醇,取一根銅絲,下端繞成螺旋狀,在酒精燈上灼燒后插入乙醇,反復幾次。注意觀察反應現象,小心地聞試管中液體產生的氣味。
現象:
在酒精燈上加熱時銅絲由 紅色變黑,插入乙醇后銅絲 又由黑變紅色。試管中液體有刺激性氣味。
氧化反應——催化氧化
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
氧化反應——催化氧化
反應原理:
2Cu+O2 2CuO
2CuO+2CH3CH2OH 2Cu + 2CH3CHO+2H2O
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
醇發生催化氧化需滿足的條件:
本碳有氫
氧化反應——催化氧化
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
【資料卡片】酗酒的危害
酒的主要成分是乙醇,少量飲酒對人體有益,但酗酒有害健康。科學研究表明酒量的大小與人體內某些酶有關。乙醇進入人體后,會在肝中通過酶的催化作用被氧化為乙醛和乙酸,最終被氧化為二氧化碳和水。過量飲酒會加重肝負擔,血液中較高濃度的乙醇和乙醛也會對人體產生毒害作用。
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
氧化反應——被強氧化劑氧化
據交警介紹,在機動車駕駛人的每100毫升血液中,酒精含量達到20毫克為飲酒駕車,大致相當于飲用一杯啤酒;每100毫升血液中酒精含量達到和超過80毫克可以認定為醉酒駕車,相當于飲用3兩低度白酒或者兩瓶啤酒。你知道酒精檢測儀的工作原理嗎?
環節三:實驗探究,突破乙醇的化學性質
乙醇的化學性質
氧化反應——被強氧化劑氧化
CH3CH2OH
乙醇
氧化
K2Cr2O7或KMnO4
CH3CHO
乙醛
氧化
K2Cr2O7或KMnO4
CH3COOH
乙酸
兩個階段:
K2Cr2O7
Cr2(SO4)3
乙醇
KMnO4(紫色)
MnSO4
(無色)
環節三:實驗探究,突破乙醇的化學性質
乙醇的用途
(1) 用作酒精燈、火鍋、內燃機等的燃料。
(2) 用作化工原料、香料、化妝品、涂料等。
(3) 醫療上常用體積分數為75%的乙醇溶液作消毒劑。
乙醇
分子組成和結構
用途
分子式
結構式
官能團
C2H6O
—OH
燃料
化工原料
醫用消毒劑
物理性質
無色、有特殊香味的液體
密度小于水
易溶于水和有機溶劑
沸點較低,易揮發
化學性質
與強氧化劑反應
氧化反應
置換反應
使酸性高錳酸鉀溶液褪色
與羥基相連的碳上必須有氫原子
淡藍色火焰
乙醇與鈉反應
環節四:歸納整理,鞏固提升
歸納整理
環節二:歸納整理,鞏固提升
鞏固提升
1.比較乙烷和乙醇的結構,下列說法錯誤的是( )
A.分子中的化學鍵都包括極性鍵和非極性鍵
B.分子中都含6個氫原子且6個氫原子的化學環境完全相同
C.乙基與1個氫原子相連就是乙烷分子
D.乙基與1個羥基相連就是乙醇分子
B
環節二:歸納整理,鞏固提升
鞏固提升
2.下列關于乙醇結構與性質的說法正確的是( )
A.乙醇分子中含有—OH,所以乙醇可溶于水,也可電離出OH-
B.乙醇能電離出H+,所以是電解質
C.乙醇與鈉反應可以產生氫氣,所以乙醇顯酸性
D.乙醇與鈉反應非常平緩,所以乙醇分子中羥基上的氫原子不如水中的
氫原子活潑
D
環節二:歸納整理,鞏固提升
鞏固提升
3.某醇在銅作催化劑的條件下和氧氣反應生成的產物為 ,
則該醇為( )
A. B.
C. D.
A
環節二:歸納整理,鞏固提升
鞏固提升
4.某化學反應過程如圖所示。由圖得出的判斷錯誤的是( )
A.生成物M的官能團為醛基
B.銅是此反應的催化劑
C. 也能發生此反應生成M的同系物
D.反應中有紅、黑交替變化的現象
C
4.某化學反應過程如圖所示。由圖得出的判斷錯誤的是( )
A.生成物M的官能團為醛基
B.銅是此反應的催化劑
C. 也能發生此反應生成M的同系物
D.反應中有紅、黑交替變化的現象
環節二:歸納整理,鞏固提升
鞏固提升
5.乙醇分子中的各種化學鍵如圖所示,關于乙醇在各種反應中斷裂鍵的說明不正確的是( )
A.和金屬鈉反應時①鍵斷裂
B.在銅催化共熱下與O2反應時斷裂①鍵和③鍵
C.在銅催化共熱下與O2反應時斷裂①鍵和⑤鍵
D.在空氣中完全燃燒時斷裂①②③④⑤鍵
C
謝謝觀看!
展開更多......
收起↑
 資源預覽
資源預覽