資源簡介
資源簡介
(共26張PPT)
1.知道氧氣的主要物理性質。
2.知道氧氣的主要化學性質
3.能用文字表達式表示化學反應,能準確描述木炭、硫、鐵絲與氧氣反應的現象。
4.知道如何判斷化合反應與氧化反應。
5.能說出氧氣的具體用途。
回顧上節課所講知識,假如你去爬雪山,你將隨身攜帶哪種氣體?為什么?
物理性質 氧氣
色、味、態 (通常狀況下)
密度 (標準狀況下)
溶解性 (通常狀況下)
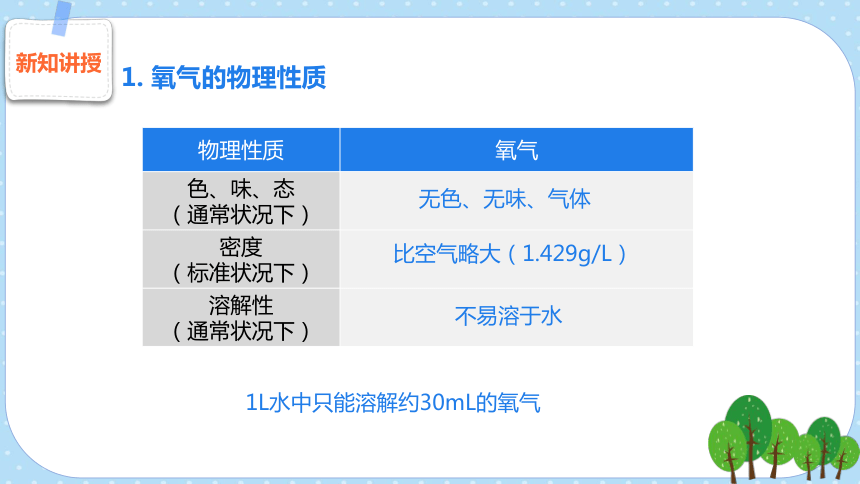
1. 氧氣的物理性質
無色、無味、氣體
比空氣略大(1.429g/L)
不易溶于水
1L水中只能溶解約30mL的氧氣
2.氧氣的三態變化
3.氧氣的貯存
氧氣 液氧 固態氧
(無色) (淡藍色液體) (淡藍色、雪花狀固體)
-183℃
-219℃
工業生產的氧氣,一般加壓貯存在藍色的鋼瓶中。(藍底黑字)
101kPa
思考與討論
如何鑒別氧氣?
物理性質:無色無味
不能鑒別
化學性質
?
空氣中的氮氣、氧氣、二氧化碳等氣體都是無色無味的
實驗1:氧氣的檢驗
實驗現象
帶火星的木條復燃。
該氣體是氧氣,氧氣能支持燃燒。
實驗結論
氧氣的化學性質:助燃性。
把帶火星的木條伸在集氣瓶中,如果帶火星的木條復燃,證明瓶里裝的是氧氣。
想一想:若要檢驗氧氣是否集滿,應如何操作?
把帶火星的木條伸在集氣瓶口,如果帶火星的木條復燃,證明瓶里裝滿氧氣。
氧氣能夠使帶火星的木條復燃。
不能使帶火星的木條復燃的氣體一定不含氧氣嗎?
使帶火星的木條復燃的氣體一定是純凈的氧氣嗎?
判斷:
復燃、不復燃等現象只能說明氣體中所含氧氣含量的相對高低,我們可以根據這個相對的高低進行進一步的判斷。
反應物名稱 顏色和 狀態 在空氣中燃燒的現象 在氧氣中燃燒的現象 文字
表達式
木炭
黑色固體
持續紅熱,放出熱量,無煙無焰,生成無色氣體
劇烈燃燒,發出白光,放出熱量,生成無色氣體
碳+氧氣 二氧化碳
C O2 CO2
點燃
木炭和氧氣的反應
木炭燃燒沒有火焰
自上而下緩慢地伸入瓶中減少氧氣的逸出,使其反應更充分。如果迅速插到瓶底,木炭主要反應下部的氧氣,而上部的氧氣會隨著產生的二氧化碳排出瓶外,導致木炭不能充分和氧氣反應。
3.氧氣的化學性質
硫和氧氣的反應
反應物名稱 顏色和 狀態 在空氣中燃燒的現象 在氧氣中燃燒的現象 文字
表達式
硫
淡黃色
固體
微弱的淡藍色火焰,放出熱量,生成有刺激性氣味的氣體
明亮的藍紫色火焰,放出熱量,生成有刺激性氣味的氣體
硫+氧氣 二氧化硫
S O2 SO2
點燃
注意:集氣瓶底部預留少量水或堿,目的是溶解吸收產生的二氧化硫,防止其逸出污染空氣。
補充:火焰、火光的區別:
火光:沸點較高的固態物質燃燒只發光;
例如:木炭在氧氣中燃燒發出白光,鐵絲在氧氣中燃燒火星四射
火焰:氣態物質或沸點較低的液體或固態物質燃燒會產生火焰。
例如:硫、蠟燭、酒精、甲烷等燃燒產生火焰
為什么木炭燃燒沒有火焰,但生活中木炭燃燒會有火焰?
反應物名 稱 顏色和狀態 在空氣中加熱的現象 在氧氣中燃燒的現象 文字表達式
鐵絲
銀白色
固體
鐵絲紅熱,
不燃燒
劇烈燃燒,火星四射,放出大量的熱,生成黑色固體
鐵+氧氣 四氧化三鐵
Fe O2 Fe3O4
點燃
鐵絲和氧氣的反應
實驗前要用砂紙打磨鐵絲,除去鐵銹
1、鐵絲為什么要盤成螺旋狀?
增大與氧氣的接觸面積便于燃燒
2、該實驗中,火柴的作用是什么?
引燃鐵絲
3、為什么火柴快燃盡時才插入瓶中?
防止火柴燃燒時消耗氧氣
4、集氣瓶底為什么要鋪上細沙或水?硫燃燒能鋪細沙嗎?
防止濺落的熔融物炸裂瓶底。不能,細沙無法吸收二氧化硫。
思考:
5、若將燒紅的鐵絲伸入集氣瓶,沒有出現鐵絲劇烈燃燒的現象,則原因可能是?
鐵銹未除去或氧氣含量低
物質在空氣中燃燒與在氧氣中燃燒的現象一樣嗎?這說明了什么?
物質在空氣中燃燒主要是與空氣中的氧氣反應,反應的劇烈程度取決于氧氣的含量,氧氣含量越高,燃燒越劇烈。
思考與討論
1、裝滿氧氣的甲乙兩個集氣瓶,按圖2-4所示,用帶火星的木條分別以甲、乙兩種方式緩緩由瓶口伸入瓶底,發現木條復燃,且在甲中比在乙中燃燒旺且時間長。上述實驗說明了氧氣具有的性質是:①______________;②___________________。
2、對氧氣的敘述錯誤的是 ( )
A.氧氣是一種無色無味的氣體
B.氧氣是能助然的氣體
C.液態氧和固態氧都是淡藍色的
D.氧氣易溶于水
氧氣具有助燃性
氧氣的密度比空氣略大
D
D
3.下列有關實驗現象的描述,正確的是( )
A.紅磷在空氣中燃燒產生大量白霧
B.木炭在空氣中燃燒生成二氧化碳
C.硫在空氣中燃燒發出藍紫色火焰
D.鐵絲在氧氣中燃燒生成黑色固體
4.下列實驗或操作中水可以用細沙代替的是 ( )
A.鐵絲在裝滿氧氣的集氣瓶中燃燒
B.硫在在裝滿氧氣的集氣瓶中燃燒
C.紅磷燃燒測定空氣中氧氣的含量
D.洗滌試管
A
反應前的物質 反應后生成的物質 反應的文字表達式
以下幾個反應中,有什么共同的特征?
碳+氧氣 二氧化碳
點燃
硫+氧氣 二氧化硫
點燃
木炭、氧氣
硫、氧氣
鐵、氧氣
二氧化碳
二氧化硫
四氧化三鐵
鐵+氧氣 四氧化三鐵
點燃
兩種反應物
一種生成物
由兩種或兩種以上的物質生成另一種物質的反應。
物質跟氧發生的反應。
氧氣在氧化反應中提供氧,它具有氧化性。
Fe O2 Fe3O4
鐵 + 氧氣 四氧化三鐵
點燃
4.化合反應
氧化反應
劇烈氧化:像燃燒那樣劇烈并發光、放熱的氧化反應。
緩慢氧化:進行得很慢,不容易被察覺的氧化反應。
A+B→AB(多變一)
緩慢氧化:進行得很慢,不容易被察覺的氧化反應叫緩慢氧化。
動植物呼吸
食物的腐爛
醋的釀造
農家肥料的腐熟
劇烈氧化 緩慢氧化
概念
舉例
區別
聯系
進行得很慢,不容易被察覺的氧化反應。
像燃燒那樣劇烈并發光、放熱的氧化反應。
木炭、硫等在氧氣中燃燒。
食物腐爛、鐵生銹等
反應現象不同,劇烈程度不同,反應條件不同
都是氧化反應,都放出熱量
所有的氧化反應都涉及發光、放熱等情況嗎?
化合反應不一定是氧化反應,氧化反應也不一定是化合反應,化合反應和氧化反應之間沒有必然的聯系。
思考:
1.氧化反應與化合反應之間存在什么關系?
2.有氧氣參與的反應一定是氧化反應嗎?
不一定。如氧氣在一定條件下可以轉化為臭氧,反應物只有氧氣,不符合氧化反應的定義。
3.氧化反應一定會發光放熱嗎?
不一定。氧化反應包括劇烈氧化和緩慢氧化。
航天員升入天空時,身上都會穿一套航天服,應急供氧裝置通過服裝軟管將氧氣送人航天服內,一部分氧氣將進入頭盔內供航天員呼吸及頭部散熱,然后由壓力調節器排出。想一想,氧氣有什么作用?
(1)供給呼吸
動植物呼吸
潛水
(2)支持燃燒
航天
氣割
氣焊
5.氧氣的用途
發酵
動植物呼吸、潛水、發酵、登山
供給呼吸(化學性質)
燃燒、航天煉鋼、氣割、氣焊等
支持燃燒(化學性質)
決定
體現
1.氧氣是一種化學性質比較活潑的氣體,它在氧化反應中提供氧,具有氧化性。下列說法正確的是( )
A.酒和醋的釀造發生了劇烈的氧化反應
B.白磷自燃既含緩慢的氧化,又包含劇烈氧化
C.蠟燭燃燒發生了化合反應
D.將帶火星的木條伸入某氣體中,若木條復燃,則證明該氣體是氧氣,木條復燃是由緩慢氧化引起的
B
2.下列化學反應中,屬于化合反應的是( ),屬于氧化反應的是( ),既是化合反應又是氧化反應的是( )
① 氫氣+氧氣
水
③酒精+氧氣
二氧化碳+水
② 水
氫氣+氧氣
④ 鐵+氧氣
四氧化三鐵
⑥二氧化碳+水
碳 酸
⑤ 磷+氧氣
五氧化二磷
①④⑤⑥
①③④⑤
①④⑤
通電
展開更多......
收起↑
 資源預覽
資源預覽