資源簡介
資源簡介
(共51張PPT)
第1章 有機化合物的結構與性質 烴
第2節 有機化合物的結構與性質
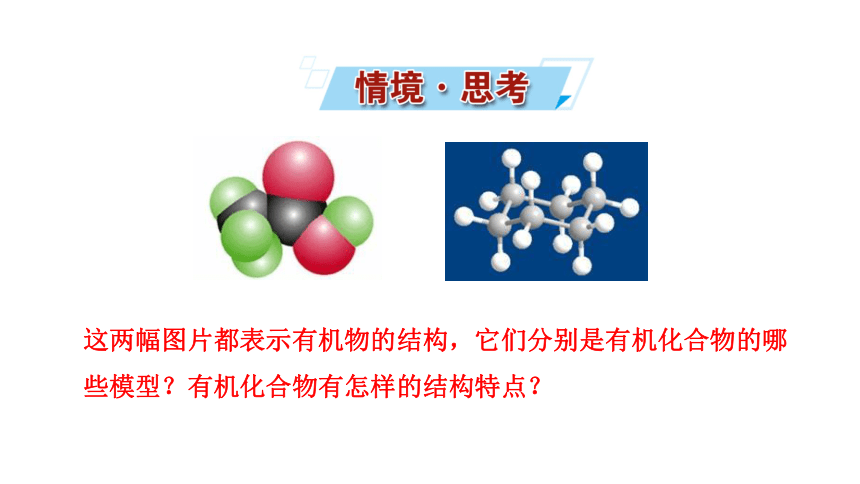
這兩幅圖片都表示有機物的結構,它們分別是有機化合物的哪些模型?有機化合物有怎樣的結構特點?
1.了解碳原子的成鍵特點和成鍵方式的多樣性,理解有機化合物種類繁多的原因。
2.了解單鍵、雙鍵、三鍵的特點,知道鍵的極性對化合物的性質的影響。
3.理解極性鍵和非極性鍵的概念,知道鍵的極性對化合物的性質的影響。
4.了解有機化合物存在的同分異構現象,能書寫和判斷簡單有機物的同分異構體。
1.認識到有機化合物的分子結構決定于原子間的連接順序、成鍵方式和空間排布,認識到有機化合物存在構造異構和立體異構等同分異構現象。能認識化學現象與模型之間的聯系,能運用多種認知模型來描述和解釋物質的結構、性質和變化。(證據推理與模型認知)
2.結合典型實例認識有機化合物分子中基團間存在相互影響,并適當開展基于結構分析預測性質和反應的學習活動。認識科學探究是進行科學解釋和發現、創造和應用的科學實踐活動,能提出有探究價值的問題,設計并優化實驗方案,完成實驗操作,能與同學交流探究成果,提出進一步探究或改進思想。(科學探究與創新意識)
體會課堂探究的樂趣,
汲取新知識的營養,
讓我們一起 吧!
進
走
課
堂
碳原子的成鍵方式
回答下列問題:
1.各有機化合物分子中與碳原子成鍵的分別是何種元素的原子?
2.各有機化合物分子中碳原子成鍵的數目分別是多少?
3.每個碳原子周圍有幾對共用電子?
C、H、O、Cl等
都是四個
四對
【思考與交流】
1.有機化合物中碳原子的成鍵特征
(1)有機化合物分子中都含有碳原子,
碳原子的最外層有 電子,
可以與其他原子形成 共價鍵。
(2)碳原子還可以彼此間以 構成碳鏈或碳環。
四個
四個
共價鍵
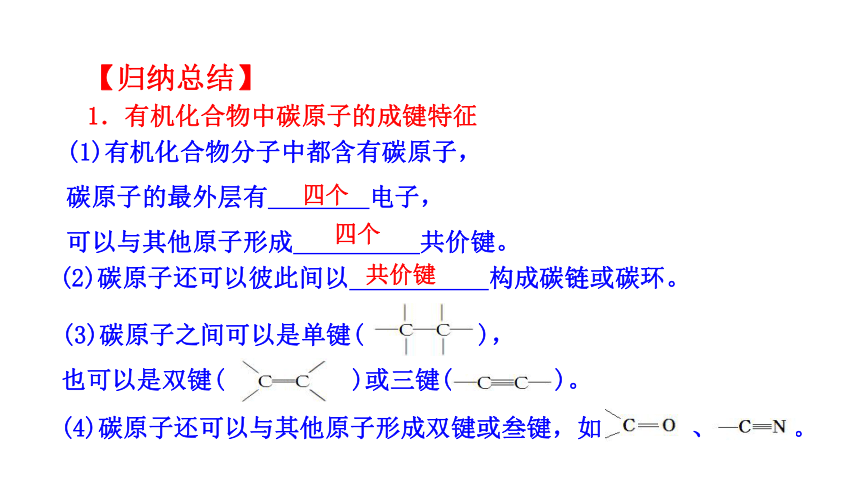
【歸納總結】
(3)碳原子之間可以是單鍵( ),
也可以是雙鍵( )或三鍵( )。
(4)碳原子還可以與其他原子形成雙鍵或叁鍵,如 、 。
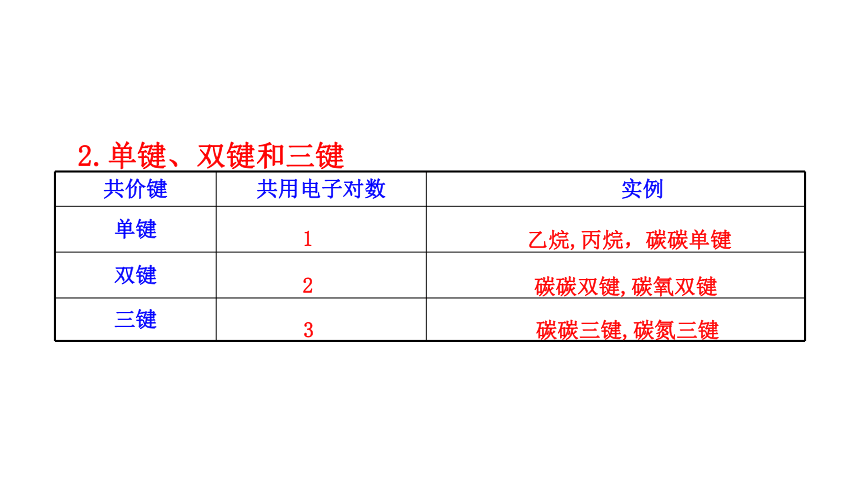
共價鍵 共用電子對數 實例
單鍵
雙鍵
三鍵
1
2
3
乙烷,丙烷,碳碳單鍵
碳碳雙鍵,碳氧雙鍵
碳碳三鍵,碳氮三鍵
2.單鍵、雙鍵和三鍵
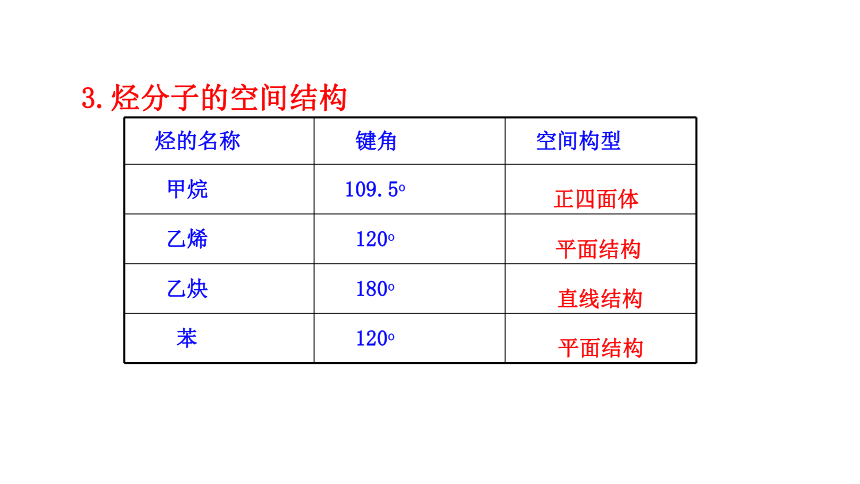
烴的名稱 鍵角 空間構型
甲烷 109.5o
乙烯 120o
乙炔 180o
苯 120o
3.烴分子的空間結構
正四面體
平面結構
直線結構
平面結構
4.極性鍵和非極性鍵
(1)極性鍵:不同元素的兩個原子成鍵時,它們吸引共用電子的能力不同,共用電子將偏向吸引電子能力較強的一方,所形成的共價鍵稱為極性鍵。
(2)非極性鍵:同種元素的兩個原子成鍵時,它們吸引共用電子的能力相同,所形成的共價鍵稱為非極性鍵。
特別強調:
極性共價鍵中,共用電子偏向的成鍵原子帶部分負電荷,共用電子偏離的成鍵原子帶部分正電荷。
非極性共價鍵中,共用電子不偏向于成鍵原子的任何一方,因此,參與成鍵的原子都不帶電荷。
根據成鍵原子吸引電子能力的差異判斷鍵的極性,進而預測有機化合物分子的反應活性和在反應中的斷鍵部位。
【歸納總結】
1. 下列物質的分子是平面結構的是 ( )
A.CH4 B.CH2 CH2 C.HC≡C—CH3 D.
【提示】有機化合物分子中,碳原子最外層有四對共用電子。若形成四個相同單鍵,如CH4,則鍵角為109°28′,為正四面體形;若形成雙鍵,鍵角為120°,如CH2 CH2,屬平面結構;若形成三鍵,鍵角為180°,如HC≡CH,屬直線形。C選項中甲基上的氫原子與其他原子不共面。
B
【學以致用】
2. CO2的資源化利用是解決溫室效應的重要途徑。以下是在一定條件下用NH3捕獲CO2生成重要化工產品三聚氰酸的反應:
3NH3+3CO2 +3H2O
(1)分子中有哪些極性共價鍵
【提示】分子中存在O—H、C—O、N—C、N C鍵,都屬于極性鍵,所以分子中不存在非極性鍵。
(2)假設六元環是和苯環一樣的平面結構,此分子中所有的原子是否一定共面
【提示】不一定。因為羥基和另外一個原子相連時是V形結構,所以所有原子不一定共面。
【學以致用】
【問題探究】
分子式為C3H8、C4H10、C5H12分別表示的是什么物質?它們的分子結構可能有幾種?
【實驗驗證】
請同學們根據自己的猜想制作分別符合分子式C3H8、C4H10、C5H12的球棍模型。
【交流成果】
分子式為C3H8、C4H10、C5H12分別表示丙烷、丁烷和戊烷。它們的分子結構分別有1種、2種、3種。
請同學們觀察C5H12的球棍模型,完成下表:
物質名稱 正戊烷 異戊烷 新戊烷
碳骨架
相同點
不同點 結構
性質
分子組成相同
碳架結構不同,出現帶有支鏈的結構
C-C-C-C-C
_
C-C-C-C
C
_
C-C-C
_
C
C
【追根究底】
物理性質不同,支鏈越多,沸點越低
1.同分異構現象:化合物具有相同的分子式,但具有不同結構的現象,叫同分異構現象。
2.同分異構體:具有同分異構現象的化合物互為同分異構體。
3.碳原子數目越多,同分異構體越多。
三同:分子式相同、分子組成相同、相對分子質量相同
兩不同:結構不同、物理性質不同
有機化合物的同分異構現象
【特別提醒】
同分異構類型
同分異構
構造異構
立體異構
碳骨架異構
官能團位置異構
官能團類型異構
順反異構
分子式相同,由_____________而產生的同分異構現象,如CH3CH2OH與______________。
同分異構類型
由________不同而產生的異構現象,如CH3CH2CH2CH3與__________互為碳架異構。
碳骨架
由官能團的______不同而產生的同分異構現象,如CH3CH2CH2OH_________。
位置
官能團不同
CH3—O—CH3
(3)官能團類型異構。
(2)官能團位置異構。
(1)碳骨架異構。
常見的官能團異構
【拓展提升】
序號
類別
通式
1
烯烴
環烷烴
2
炔烴
二烯烴
3
飽和一元鏈狀醇
飽和醚
4
飽和一元鏈狀醛
酮
5
飽和羧酸
酯
C
n
H
2n
C
n
H
2n
-
2
C
n
H
2n+2
O
C
n
H
2n
O
C
n
H
2n
O
2
6
氨基酸、硝基化合物
C
n
H
2n+1
NO
2
1.互稱為同分異構體的物質不可能( )
A.具有相同的相對分子質量
B.具有相同熔、沸點和密度
C.具有相同的分子式
D.具有相同的組成元素
B
【即時鞏固】
【提示】同分異構體即分子式相同(相對分子質量相同,組成元素也相同),但結構不同,因此其物理性質不可能完全相同。
(1)1-丙醇和2-丙醇 _____________
(2)CH3COOH和HCOOCH3 _____________
(3)CH3CH2CHO和CH3COCH3 _____________
(4)CH3-CH(CH3)2和CH3-CH2-CH2-CH3 _____________
(5)CH3CH=CHCH2CH3和CH2=CHCH2CH2CH3 __________________
2.下列異構屬于何種異構?
位置異構
類型異構
類型異構
碳骨架異構
位置異構
C=C
H3C
H
CH3
H
C=C
H3C
CH3
H
H
二者的結構一樣嗎?
和
烯烴的順反異構
烯烴的順反異構
①定義:當碳碳雙鍵的兩個碳原子所連的其他兩個原子或原子團不同時,就會產生順反異構現象。
②產生順反異構體的條件:
1. 具有碳碳雙鍵
2. 組成雙鍵的每個碳原子必須連接兩個不同的原子或原子團。
有順反異構的類型
無順反異構的類型
順-2-丁烯
反-2-丁烯
以2-丁烯為例:
相同的原子或原子團位于雙鍵同一側為順式結構
相同的原子或原子團位于雙鍵兩側為反式結構
C
C
CH3
CH3
H
H
C
C
CH3
CH3
H
H
【拓展提高1】烷烴的同分異構體的書寫
【挑戰自我】
以C7H16為例,寫出它的同分異構體。
【成果交流】
寫出C7H16的同分異構體以后與其他同學交流:你是用什么方法寫出來的?有沒有重復的情況?有沒有漏寫的情況?
以C7H16為例,寫出它們的同分異構體。
(1)最長碳鏈
H
H
H
H
H
H
H
H
H
C
C
C
C
-
-
-
-
-
∣
∣
∣
∣
∣
∣
∣
∣
C
C
C
-
-
∣
∣
∣
∣
∣
∣
-
H
H
H
H
H
H
H
同分異構體的書寫方法
——降碳對稱法(適用于碳架異構)
(2)從直鏈上去掉一個-CH3,依次連在剩余碳鏈中心對稱線一側的各個碳原子上。甲基可連在2,3號碳上: , 根據碳鏈中心對稱,將-CH3連在對稱軸的右側會與左側連接方式重復。
3
1
2
C-C-C-C-C-C
(3)再從主鏈上去掉一個碳,可以形成一個-CH2CH3或兩個-CH3,主鏈變為 。當取代基為-CH2CH3時,由于對稱關系只能連在3號碳上。當取代基為兩個-CH3時,在主鏈上先定一個甲基,按照位置由近至遠的順序移動另一個甲基,注意不要重復。即兩個甲基可分別在2和2、2和3、2和4、3和3上。
4
3
1
2
C-C-C-C-C
5
降碳對稱法規律口訣
主鏈由長到短;
減碳架作支鏈;
支鏈由整到散;
位置由心到邊;
排布由對到鄰再到間;
最后用氫原子補足碳原子的四個價鍵。
【拓展提高2】
【挑戰自我】
以分子式為C5H12O的醇為例,寫出它的同分異構體。
【成果交流】
寫出分子式為C5H12O的醇的同分異構體,與其他同學交流:是用什么方法寫出來的?所寫的同分異構體有沒有重復現象?有沒有漏寫現象?
醇的同分異構體的書寫
先碳骨架異構,后位置異構。
如書寫分子式為C5H12O的醇的同分異構體。
(1)先寫出C5H12的同分異構體為
3
1
2
C-C-C-C-C
C-C-C-C
4
6
5
C
7
8
C-C-C
C
C
(2)再用-OH取代圖中標有數字的碳上的氫原子,故共有8種。
同分異構體的書寫方法
——取代法(適用于醇、鹵代烴異構體書寫)
1.已知丙烷的二氯代物有四種異構體,則其六氯代物的異構體數目為( )
A.兩種 B.三種 C.四種 D.五種
【提示】采用換元法,將氯原子代替氫原子,氫原子代替氯原子,從二氯代物有四種同分異構體,就可得到六氯代物也有四種同分異構體。
C
【學以致用】
2.判斷下列說法的正誤:
(1)氰酸(H—O—C≡N)和雷酸(H—N==C==O)都是
無機物,它們不屬于同分異構體。( )
(2)分子式為C4H10的烷烴一定為純凈物。( )
(3)分子式為C5H11Cl的同分異構體共有7種。( )
(4)分子式為C3H6Cl2的同分異構體共有4種。( )
√
×
×
×
先根據給定的碳原子數寫出烷烴的同分異構體的碳骨架,再將官能團插入碳鏈中。
如書寫分子式為C4H8的烯烴的同分異構體(插入雙鍵),雙鍵可以分別在1、2、3號位置上。
2
1
C-C-C-C
3
C-C-C
C
同分異構體的書寫方法
——插入法(適用于烯烴、炔烴、酯等)
種 類 表 示 方 法 實 例
分子式
最簡式
(實驗式)
電子式
有機物分子結構的表示方法
用元素符號表示物質的分子組成,書寫時將同種元素的原子合并到一起
CH4、C3H6
表示物質組成的各元素原子的最簡整數比
乙烯最簡式為CH2,
C6H12O6最簡式為CH2O
用小黑點或“×”號表示原子最外層電子的成鍵情況
C
H
H
H
H
×·
·×
·
×
×
·
【資料卡片】
種 類 表 示 方 法 實 例
結構式
結構
簡式
用短線“—”來表示1個共價鍵,用“—”(單鍵)“=”(雙鍵)或“≡”(三鍵)將所有原子連接起來
H—C=C—H
H
H
①表示單鍵的“—”可以省略,將與碳原子相連的其他原子寫在其旁邊,在右下角注明其個數
②表示碳碳雙鍵、碳碳三鍵的“=”“≡”不能省略
③醛基( )、羧基( )
可簡化成—CHO、—COOH
—C—H
O
—C—OH
O
CH3CH=CH2、
CH3CH2OH、
HC—COOH
O
種 類 表 示 方 法 實 例
鍵 線 式
球棍
模型
比例
模型
①進一步省去碳氫元素的符號,只要求表示出碳碳鍵以及與碳原子相連的基團
②圖示中的每個拐點、起點和終點均表示一個碳原子,每一條線段代表一個共價鍵,每個碳原子都形成四個共價鍵,不足的用氫原子補足
小球表示原子,短棍表示價鍵
用不同體積的小球表示分子中原子的結合情況
可表示為:
CH3
CH3CH=CHCHCH3
【拓展視野】
對映異構
對映異構:存在于手性分子中
手性分子:如果一對分子,它們的組成和原子的排列方式完全相同,但如同左手和右手一樣互為鏡像,在三維空間里不能重疊,這對分子互稱為手性異構體。有手性異構體的分子稱為手性分子。(分子內能找到對稱軸或對稱中心的分子為非手性的)
丙氨酸的對映異構體模型
什么樣的有機物才能有對映異構?
CH3—CH—CH2—CH3
OH
*
一般情況下,分子有無手性往往與分子中是否含有手性碳原子有關。
飽和碳原子上連接四個不同的原子或基團的碳原子,
常用“*”號予以標注。
*
*
【思考與討論】
手性碳原子:
CH3—CH—CH—CH3
Cl
Br
三、有機化合物結構與性質的關系
已知有機化合物的結構如何預測其性質?
分析結構
找出官能團
鍵的極性及碳原子的飽和程度
預測性質
【思考與交流】
(1)乙酸分子中存在-COOH,哪些性質反映了它的結構特點?
乙酸的酸性、乙酸與醇的酯化反應
(2)乙酸和乙醇中都有-OH,但二者的化學性質不同,為什么?
與-OH相連的其他基團不同
【交流·研討】
1.官能團與有機化合物性質的關系
(1)官能團中含有極性強的鍵易發生相關的化學反應,例如,醇的官能團是羥基(-OH),羥基有很強的極性,導致醇類表現出一定的特性。
(2)官能團中含有不飽和碳原子,易發生相關的化學反應。例如乙烯、乙炔分子中含有不飽和鍵,可以與其他原子或原子團結合成新的產物,使其化學性質比烷烴的活潑。
【歸納總結】
2.不同基團的相互影響與有機化合物性質的關系
(1)苯和甲苯都含有苯環,但與濃硝酸發生反應條件不同。
(2)乙酸和乙醇都含有羥基,但化學性質差別很大。
(3)乙醇和苯酚都含有羥基,但化學性質差別很大。
(4)醛和酮都含有羰基,但化學性質差別很大。
立體異構
順反異構
對映異構
官能團異構
·······
通式相同的物質
烯烴部分繼續學習
手性碳原子的判斷
構造異構
碳架異構
位置異構
降碳對稱法
插入法
換元法
同分異構現象
(1)有機化合物中的官能團決定其性質。
(2)與官能團相連基團的不同決定了具有相同官能團的有機化合物的性質有所不同。
有機化合物結構與性質的關系
1.下列物質分子中,屬于正四面體結構的是( )
A.CCl4 B.CHCl3
C.CH2Cl2 D.CH3Cl
A
【提示】由甲烷分子的正四面體結構推知CCl4應該也是正四面體結構。
2.環之間共用一個碳原子的化合物稱為螺環化合物,螺[2.2]戊烷
( )是最簡單的一種。下列關于該化合物的說法錯誤的是( )
A.與環戊烯互為同分異構體
B.二氯代物超過兩種
C.所有碳原子均處同一平面
D.生成1 mol C5H12至少需要2 mol H2
D
3.下列烷烴進行一氯取代反應后,只能生成三種沸點不同的有機物
的烷烴是( )
A.(CH3)2CHCH2CH2CH3 B.(CH3CH2)2CHCH3
C.(CH3)2CHCH(CH3)2 D.(CH3)3CCH2CH3
【提示】生成三種沸點不同的有機物,說明此烷烴一氯取代后生成三種同分異構體,根據各選項的等效氫原子種數判斷,A項有5種,B項有4種,C項有2種,D項有3種。
D
4.(雙選)下列關于CH3—CH=CH—C≡C—CF3分子
的結構敘述正確的是( )
A.6個碳原子有可能都在一條直線上
B.6個碳原子不可能都在一條直線上
C.6個碳原子一定都在同一平面上
D.6個碳原子不可能都在同一平面上
BC
F
H
F
5.下列各組物質中,哪些屬于同分異構體,是同分異構體的屬于何種異構?
①H2N—CH2—COOH和H3C—CH2—NO2
②CH3CH2COOH和CH3COOCH3
③CH3CH2CH2CHO和CH3COCH2CH3
④CH3CH2CH2OH和CH3CH2OCH3
【提示】①②③④中兩物質均為同分異構體,均屬于官能團異構。
6.寫出分子式為C6H14的有機物的所有同分異構體的結構簡式。
【提示】
展開更多......
收起↑
 資源預覽
資源預覽